Volně prodejný léčivý přípravek - Extrakt z listů jinanu dvoulaločného. PŘÍBALOVÁ INFORMACEPŘÍBALOVÁ INFORMACE: INFORMACE PRO UŽIVATELE TEBOKAN 120 mg Potahované tablety Ginkgonis extractum siccum raffinatum et quantificatum (EGb 761) Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje. Vždy užívejte tento přípravek přesně v souladu s příbalovou informací nebo podle pokynů svého lékaře nebo lékárníka. - Ponechte si příbalovou... Celý popis
Koupit za 349 Kč- Od nejoblíbenějších
- Od nejlevnějších
- Od nejdražších
 98 %
98 %
Tebokan 120mg 30 tablet
Doprava:
59 Kč
Skladem
427 Kč
Koupit za 427 Kč
 100 %
100 %
Tebokan 120mg por.tbl.flm. 30x120mg
Doprava:
59 Kč
Skladem
413 Kč
Koupit za 413 Kč
 98 %
98 %
Tebokan 120mg por.tbl.flm. 30x120mg
Doprava:
zdarma
Skladem
411 Kč
Koupit za 411 Kč
 100 %
100 %
TEBOKAN POR 120MG TBL FLM 30
Doprava:
95 Kč
Skladem
410 Kč
Koupit za 410 Kč
 93 %
93 %
Tebokan 120mg por.tbl.flm. 30x120mg
Doprava:
59 Kč
Skladem
408 Kč
Koupit za 408 Kč
Popis
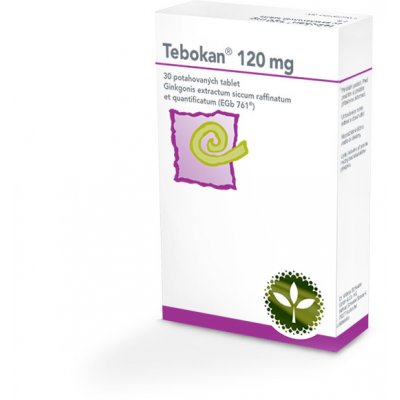
Volně prodejný léčivý přípravek - Extrakt z listů jinanu dvoulaločného. PŘÍBALOVÁ INFORMACEPŘÍBALOVÁ INFORMACE:
INFORMACE PRO UŽIVATELE TEBOKAN 120 mg Potahované tablety Ginkgonis extractum siccum raffinatum et quantificatum (EGb 761)
Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
Vždy užívejte tento přípravek přesně v souladu s příbalovou informací nebo podle pokynů svého lékaře nebo lékárníka.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Požádejte svého lékaře nebo lékárníka, pokud potřebujete další informace nebo radu.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, viz bod 4.
- Pokud se do 8 týdnů nebudete cítit lépe nebo pokud se Vám přitíží, musíte se poradit s lékařem.
-
Co naleznete v této příbalové informaci:
1. Co je TEBOKAN 120 mg a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete TEBOKAN 120 mg užívat 3. Jak se TEBOKAN 120 mg užívá 4. Možné nežádoucí účinky 5 Jak TEBOKAN 120 mg uchovávat 6. Obsah balení a další informace
1. CO JE TEBOKAN 120 mg A K ČEMU SE POUŽÍVÁ
TEBOKAN 120 mg obsahuje Ginkgonis extractum siccum raffinatum et quantificatum 35 - 67:1, extrahováno acetonem 60% m/m, což odpovídá 26,4 - 32,4 mg flavonových glykosidů a 6,48 – 7,92 mg terpenolaktonů, extrakt EGb 761 z listů jinanu dvoulaločného (Ginkgo biloba), který má účinek vazodilatační (cévy rozšiřující) v tepenné oblasti a reologický (zlepšuje průtokové vlastnosti krve). Snížením kapilární propustnosti (permeability) působí lehce protiedémově (proti otokům). Podporuje žilní tonus (napětí), zlepšuje využití glukózy v buňkách a snižuje tvorbu a přítomnost nežádoucích produktů vznikajících při metabolismu (tzv. volných kyslíkových radikálů). Přípravek zvyšuje syntézu a uvolňování substance nazývající se acetylcholin, jejíž množství je ve stáří sníženo.
Bez porady s lékařem se přípravek užívá
- při poruchách duševní výkonnosti s příznaky: poruchy paměti, poruchy koncentrace, emoční labilita hlavně u starších osob.
Po poradě s lékařem se dále přípravek užívá
- při syndromu demence (primární degenerativní demence Alzheimerova typu, vaskulární demence, smíšené formy demence), jejímiž hlavními příznaky jsou poruchy paměti, poruchy koncentrace, deprese, závratě, tinitus (ušní šelest), bolesti hlavy.
- při poruchách prokrvení končetin jako je okluzivní choroba periferních tepen ve stadiu I.-II. podle Fontaina (projevující se jako bolest vznikající při chůzi, tzv. claudicatio intermittens),
- při senzorických (smyslových) poruchách cévního původu, jako je: závrať, ušní šelest (tinitus).
2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE TEBOKAN 120 mg UŽÍVAT
Neužívejte TEBOKAN 120 mg
- jestliže jste alergický/á na extrakt z listů jinanu dvoulaločného (Ginkgo biloba) nebo na kteroukoli další složku léku TEBOKAN 120 mg (uvedenou v bodě 6).
Upozornění a opatření
Než začnete užívat Tebokan 120 mg, poraďte se s lékařem:
- v případě zvýšeného sklonu ke spontánnímu krvácení (hemoragická diatéza) a v případě současného užívání antikoagulačních léků (léky, které zabraňují srážení krve), by měl být Tebokan 120 mg užíván pouze po konzultaci s lékařem, neboť nelze vyloučit, že přípravky obsahující Ginkgo by mohly zvýšit sklon ke krvácení.
- Pokud trpíte epileptickými záchvaty, prosím konzultujte léčbu přípravkem Tebokan 120 mg se svým lékařem, než začnete s jeho užíváním.
- Pokud trpíte depresivní náladou a bolestmi hlavy, které se nevyskytují v souvislosti se syndromem demence. Váš lékař rozhodne o vhodnosti užívání Tebokanu 120 mg.
Děti a dospívající
Vzhledem k tomu, že nejsou dostatečné údaje o bezpečnosti týkající se užívání tohoto léčivého přípravku u dětí, neměl by být tento přípravek užíván u dětí a dospívajících mladších 18 let.
Další léčivé přípravky a Tebokan 120 mg
Žádné klinicky významné interakce nejsou dosud známy.
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.. Těhotenství, kojení a plodnost
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Jelikož nejsou k dispozici dostatečné informace týkající se bezpečnosti užívání přípravku v průběhu těhotenství a kojení, nedoporučuje se tento přípravek užívat během těhotenství a kojení. Není známo, zda jsou složky přípravku vylučovány do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Žádné účinky na schopnost řídit a obsluhovat stroje nebyly hlášeny.
.
TEBOKAN 120 mg potahované tablety obsahuje monohydrát laktózy. Pokud Vám Váš lékař řekl, že nesnášíte některé cukry, poraďte se se svým lékařem, než začnete tento léčivý přípravek užívat.
3. JAK SE TEBOKAN 120 mg UŽÍVÁ
Vždy užívejte tento přípravek přesně v souladu s příbalovou informací nebo podle pokynů svého lékaře či lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Léčba bez porady s lékařem:
Při poruchách duševní výkonnosti:
Pro dospělé starší 18 let je obvyklá dávka 1 - potahovaná tableta denně (což odpovídá 120 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně). Délka léčby: Délka léčby závisí na závažnosti příznaků a měla by trvat nejméně 8 týdnů. Pokud se Vaše příznaky zhorší nebo nezlepší do 8 týdnů, vyhledejte lékaře. Bez porady s lékařem neužívejte Tebokan 120 mg déle než 3 měsíce. Po třech měsících se poraďte s lékařem nebo lékárníkem, zda je nutné pokračovat v léčbě.
Léčba po poradě s lékařem:
Při syndromu demence /typy viz výše/:
Pro dospělé starší 18 let je obvyklá dávka 1 - 2 potahované tablety denně (což odpovídá 120 - 240 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně).
Délka léčby: Délka léčby závisí na závažnosti příznaků, minimální doba léčby by měla být nejméně 8 týdnů. Po tříměsíční terapii Váš lékař posoudí přínos pokračování v léčbě.
Při poruchách prokrvení končetin a při senzorických (smyslových) poruchách (závrať, ušní šelest):
Obvyklé dávkování je 1 potahovaná tableta denně (což odpovídá 120 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně).
Délka léčby: Při poruchách prokrvení končetin by měl být lék užíván minimálně po dobu 6 týdnů, teprve pak dojde k prodloužení úseku, který nemocný dokáže ujít s úlevou od bolesti. Při léčbě vertiga (závrať) a tinitu (ušní šelest) léčba delší než 6-8 týdnů nepřináší další léčebný prospěch.
Váš lékař Vám řekne, jak dlouho máte tento lék užívat.
Způsob užívání: Potahované tablety by měly být užívány nerozkousané s malým množstvím vody. Tebokan 120 mg se užívá nezávisle na jídle.
Použití u dětí a dospívajících
Jelikož nejsou dostatečné údaje o bezpečnosti týkající se užívání tohoto léčivého přípravku u dětí a dospívajících, Tebokan 120 mg se nedoporučuje podávat dětem a dospívajícím mladším 18 let.
Jestliže jste užil(a) více Tebokanu 120 mg, než jste měl(a) Předávkování nebylo dosud zaznamenáno.
Jestliže jste zapomněl(a) užít TEBOKAN 120 mg Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku, ale pokračujte
v užívání tak, jak je napsané v této příbalové informaci. Jestliže jste přestal(a) užívat TEBOKAN 120 mg Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY
Podobně jako všechny léky, může mít i TEBOKAN 120 mg nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Nejsou žádné ověřené údaje týkající se frekvence nežádoucích účinků pozorovaných při léčbě přípravky obsahujícími Ginkgo biloba, jelikož tyto nežádoucí účinky jsou známy z jednotlivých hlášení pacientů, lékařů nebo lékárníků. Podle těchto hlášení se mohou při léčbě Tebokanem 120 mg vyskytnout následující vedlejší příznaky: bolesti hlavy, krvácení z jednotlivých orgánů, mírné gastrointestinální potíže, kožní alergické reakce (zčervenání, otok, svědění).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
www.sukl.cz/nahlasit-nezadouci-ucinek
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. JAK TEBOKAN 120 mg UCHOVÁVAT
Tento přípravek nevyžaduje speciální podmínky pro uchovávání. Uchovávejte mimo dohled a dosah dětí. TEBOKAN 120 mg nepoužívejte po uplynutí doby použitelnosti, uvedené na krabičce a blistru za označením Použitelné do/EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Nevyhazujte žádné léčivé do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. OBSAH BALENÍ A DALŠÍ INFORMACE
Co TEBOKAN 120 mg obsahuje
Léčivou látkou je: Ginkgonis extractum siccum raffinatum et quantificatum 35 - 67:1, extrahováno acetonem 60% m/m, což odpovídá 26,4 - 32,4 mg flavonových glykosidů a 6,48 – 7,92 mg terpenolaktonů v množství 120 mg v 1 potahované tabletě.
Pomocnými látkami jsou: sodná sůl kroskarmelózy, koloidní bezvodý oxid křemičitý, hypromelóza, monohydrát laktózy, makrogol 1500, magnesium-stearát, kukuřičný škrob, mikrokrystalická celulóza, protipěnivá silikonová emulze vysušená, mastek, oxid titaničitý E 171, červený oxid železitý E 172.
Jak TEBOKAN 120 mg vypadá a co obsahuje toto balení
TEBOKAN 120 mg je červená, kulatá, hladká potahovaná tableta. TEBOKAN 120 mg je dostupný v balení po 20, 30, 50, 60, 90, 100, 120 a 150 potahovaných tabletách. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Dr. Willmar Schwabe GmbH & Co. KG Willmar-Schwabe-Str. 4 D-76227 Karlsruhe
Německo
Tel.: 0049 721 4005 0
Fax: 0049 721 4005 202
Email: info@schwabepharma.com
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Schwabe Czech Republic s.r.o.
Čestmírova 1
140 00 Praha 4
Česká republika
Tel: +420 241 740 447
email: info@schwabe.cz
Tato příbalová informace byla naposledy revidována : 4.2.2015
INFORMACE PRO UŽIVATELE TEBOKAN 120 mg Potahované tablety Ginkgonis extractum siccum raffinatum et quantificatum (EGb 761)
Přečtěte si pozorně tuto příbalovou informaci dříve, než začnete tento přípravek užívat, protože obsahuje pro Vás důležité údaje.
Vždy užívejte tento přípravek přesně v souladu s příbalovou informací nebo podle pokynů svého lékaře nebo lékárníka.
- Ponechte si příbalovou informaci pro případ, že si ji budete potřebovat přečíst znovu. - Požádejte svého lékaře nebo lékárníka, pokud potřebujete další informace nebo radu.
- Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci, viz bod 4.
- Pokud se do 8 týdnů nebudete cítit lépe nebo pokud se Vám přitíží, musíte se poradit s lékařem.
-
Co naleznete v této příbalové informaci:
1. Co je TEBOKAN 120 mg a k čemu se používá 2. Čemu musíte věnovat pozornost, než začnete TEBOKAN 120 mg užívat 3. Jak se TEBOKAN 120 mg užívá 4. Možné nežádoucí účinky 5 Jak TEBOKAN 120 mg uchovávat 6. Obsah balení a další informace
1. CO JE TEBOKAN 120 mg A K ČEMU SE POUŽÍVÁ
TEBOKAN 120 mg obsahuje Ginkgonis extractum siccum raffinatum et quantificatum 35 - 67:1, extrahováno acetonem 60% m/m, což odpovídá 26,4 - 32,4 mg flavonových glykosidů a 6,48 – 7,92 mg terpenolaktonů, extrakt EGb 761 z listů jinanu dvoulaločného (Ginkgo biloba), který má účinek vazodilatační (cévy rozšiřující) v tepenné oblasti a reologický (zlepšuje průtokové vlastnosti krve). Snížením kapilární propustnosti (permeability) působí lehce protiedémově (proti otokům). Podporuje žilní tonus (napětí), zlepšuje využití glukózy v buňkách a snižuje tvorbu a přítomnost nežádoucích produktů vznikajících při metabolismu (tzv. volných kyslíkových radikálů). Přípravek zvyšuje syntézu a uvolňování substance nazývající se acetylcholin, jejíž množství je ve stáří sníženo.
Bez porady s lékařem se přípravek užívá
- při poruchách duševní výkonnosti s příznaky: poruchy paměti, poruchy koncentrace, emoční labilita hlavně u starších osob.
Po poradě s lékařem se dále přípravek užívá
- při syndromu demence (primární degenerativní demence Alzheimerova typu, vaskulární demence, smíšené formy demence), jejímiž hlavními příznaky jsou poruchy paměti, poruchy koncentrace, deprese, závratě, tinitus (ušní šelest), bolesti hlavy.
- při poruchách prokrvení končetin jako je okluzivní choroba periferních tepen ve stadiu I.-II. podle Fontaina (projevující se jako bolest vznikající při chůzi, tzv. claudicatio intermittens),
- při senzorických (smyslových) poruchách cévního původu, jako je: závrať, ušní šelest (tinitus).
2. ČEMU MUSÍTE VĚNOVAT POZORNOST, NEŽ ZAČNETE TEBOKAN 120 mg UŽÍVAT
Neužívejte TEBOKAN 120 mg
- jestliže jste alergický/á na extrakt z listů jinanu dvoulaločného (Ginkgo biloba) nebo na kteroukoli další složku léku TEBOKAN 120 mg (uvedenou v bodě 6).
Upozornění a opatření
Než začnete užívat Tebokan 120 mg, poraďte se s lékařem:
- v případě zvýšeného sklonu ke spontánnímu krvácení (hemoragická diatéza) a v případě současného užívání antikoagulačních léků (léky, které zabraňují srážení krve), by měl být Tebokan 120 mg užíván pouze po konzultaci s lékařem, neboť nelze vyloučit, že přípravky obsahující Ginkgo by mohly zvýšit sklon ke krvácení.
- Pokud trpíte epileptickými záchvaty, prosím konzultujte léčbu přípravkem Tebokan 120 mg se svým lékařem, než začnete s jeho užíváním.
- Pokud trpíte depresivní náladou a bolestmi hlavy, které se nevyskytují v souvislosti se syndromem demence. Váš lékař rozhodne o vhodnosti užívání Tebokanu 120 mg.
Děti a dospívající
Vzhledem k tomu, že nejsou dostatečné údaje o bezpečnosti týkající se užívání tohoto léčivého přípravku u dětí, neměl by být tento přípravek užíván u dětí a dospívajících mladších 18 let.
Další léčivé přípravky a Tebokan 120 mg
Žádné klinicky významné interakce nejsou dosud známy.
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.. Těhotenství, kojení a plodnost
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Jelikož nejsou k dispozici dostatečné informace týkající se bezpečnosti užívání přípravku v průběhu těhotenství a kojení, nedoporučuje se tento přípravek užívat během těhotenství a kojení. Není známo, zda jsou složky přípravku vylučovány do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Žádné účinky na schopnost řídit a obsluhovat stroje nebyly hlášeny.
.
TEBOKAN 120 mg potahované tablety obsahuje monohydrát laktózy. Pokud Vám Váš lékař řekl, že nesnášíte některé cukry, poraďte se se svým lékařem, než začnete tento léčivý přípravek užívat.
3. JAK SE TEBOKAN 120 mg UŽÍVÁ
Vždy užívejte tento přípravek přesně v souladu s příbalovou informací nebo podle pokynů svého lékaře či lékárníka. Pokud si nejste jistý(á), poraďte se se svým lékařem nebo lékárníkem.
Léčba bez porady s lékařem:
Při poruchách duševní výkonnosti:
Pro dospělé starší 18 let je obvyklá dávka 1 - potahovaná tableta denně (což odpovídá 120 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně). Délka léčby: Délka léčby závisí na závažnosti příznaků a měla by trvat nejméně 8 týdnů. Pokud se Vaše příznaky zhorší nebo nezlepší do 8 týdnů, vyhledejte lékaře. Bez porady s lékařem neužívejte Tebokan 120 mg déle než 3 měsíce. Po třech měsících se poraďte s lékařem nebo lékárníkem, zda je nutné pokračovat v léčbě.
Léčba po poradě s lékařem:
Při syndromu demence /typy viz výše/:
Pro dospělé starší 18 let je obvyklá dávka 1 - 2 potahované tablety denně (což odpovídá 120 - 240 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně).
Délka léčby: Délka léčby závisí na závažnosti příznaků, minimální doba léčby by měla být nejméně 8 týdnů. Po tříměsíční terapii Váš lékař posoudí přínos pokračování v léčbě.
Při poruchách prokrvení končetin a při senzorických (smyslových) poruchách (závrať, ušní šelest):
Obvyklé dávkování je 1 potahovaná tableta denně (což odpovídá 120 mg extraktu z listů jinanu dvoulaločného (Ginkgo biloba) denně).
Délka léčby: Při poruchách prokrvení končetin by měl být lék užíván minimálně po dobu 6 týdnů, teprve pak dojde k prodloužení úseku, který nemocný dokáže ujít s úlevou od bolesti. Při léčbě vertiga (závrať) a tinitu (ušní šelest) léčba delší než 6-8 týdnů nepřináší další léčebný prospěch.
Váš lékař Vám řekne, jak dlouho máte tento lék užívat.
Způsob užívání: Potahované tablety by měly být užívány nerozkousané s malým množstvím vody. Tebokan 120 mg se užívá nezávisle na jídle.
Použití u dětí a dospívajících
Jelikož nejsou dostatečné údaje o bezpečnosti týkající se užívání tohoto léčivého přípravku u dětí a dospívajících, Tebokan 120 mg se nedoporučuje podávat dětem a dospívajícím mladším 18 let.
Jestliže jste užil(a) více Tebokanu 120 mg, než jste měl(a) Předávkování nebylo dosud zaznamenáno.
Jestliže jste zapomněl(a) užít TEBOKAN 120 mg Nezdvojnásobujte následující dávku, abyste nahradil(a) vynechanou dávku, ale pokračujte
v užívání tak, jak je napsané v této příbalové informaci. Jestliže jste přestal(a) užívat TEBOKAN 120 mg Máte-li jakékoli další otázky, týkající se užívání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
4. MOŽNÉ NEŽÁDOUCÍ ÚČINKY
Podobně jako všechny léky, může mít i TEBOKAN 120 mg nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Nejsou žádné ověřené údaje týkající se frekvence nežádoucích účinků pozorovaných při léčbě přípravky obsahujícími Ginkgo biloba, jelikož tyto nežádoucí účinky jsou známy z jednotlivých hlášení pacientů, lékařů nebo lékárníků. Podle těchto hlášení se mohou při léčbě Tebokanem 120 mg vyskytnout následující vedlejší příznaky: bolesti hlavy, krvácení z jednotlivých orgánů, mírné gastrointestinální potíže, kožní alergické reakce (zčervenání, otok, svědění).
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
www.sukl.cz/nahlasit-nezadouci-ucinek
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5. JAK TEBOKAN 120 mg UCHOVÁVAT
Tento přípravek nevyžaduje speciální podmínky pro uchovávání. Uchovávejte mimo dohled a dosah dětí. TEBOKAN 120 mg nepoužívejte po uplynutí doby použitelnosti, uvedené na krabičce a blistru za označením Použitelné do/EXP. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Nevyhazujte žádné léčivé do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí. 6. OBSAH BALENÍ A DALŠÍ INFORMACE
Co TEBOKAN 120 mg obsahuje
Léčivou látkou je: Ginkgonis extractum siccum raffinatum et quantificatum 35 - 67:1, extrahováno acetonem 60% m/m, což odpovídá 26,4 - 32,4 mg flavonových glykosidů a 6,48 – 7,92 mg terpenolaktonů v množství 120 mg v 1 potahované tabletě.
Pomocnými látkami jsou: sodná sůl kroskarmelózy, koloidní bezvodý oxid křemičitý, hypromelóza, monohydrát laktózy, makrogol 1500, magnesium-stearát, kukuřičný škrob, mikrokrystalická celulóza, protipěnivá silikonová emulze vysušená, mastek, oxid titaničitý E 171, červený oxid železitý E 172.
Jak TEBOKAN 120 mg vypadá a co obsahuje toto balení
TEBOKAN 120 mg je červená, kulatá, hladká potahovaná tableta. TEBOKAN 120 mg je dostupný v balení po 20, 30, 50, 60, 90, 100, 120 a 150 potahovaných tabletách. Na trhu nemusí být všechny velikosti balení.
Držitel rozhodnutí o registraci a výrobce
Dr. Willmar Schwabe GmbH & Co. KG Willmar-Schwabe-Str. 4 D-76227 Karlsruhe
Německo
Tel.: 0049 721 4005 0
Fax: 0049 721 4005 202
Email: info@schwabepharma.com
Další informace o tomto přípravku získáte u místního zástupce držitele rozhodnutí o registraci:
Schwabe Czech Republic s.r.o.
Čestmírova 1
140 00 Praha 4
Česká republika
Tel: +420 241 740 447
email: info@schwabe.cz
Tato příbalová informace byla naposledy revidována : 4.2.2015
Parametry
| Výrobce | Dr. Willmar Schwabe |
| Příznaky | poruchy paměti a demence. poru |
| Forma přípravku | tablety |
| Určení | univerzální |
| Množství | 30 ks |
| Značka | Tebokan |
| Věk | pro dospělé |
| Hmotnost | 0 g |
| Příchuť | ne |